Enzym HRP do ELISA: przewodnik po pozyskiwaniu enzymów diagnostycznych
Pozyskaj enzym HRP klasy diagnostycznej do ELISA wraz ze wskazówkami dotyczącymi specyfikacji, QC, dopasowania do procesu oraz przeglądu COA/TDS/SDS i kwalifikacji dostawcy.
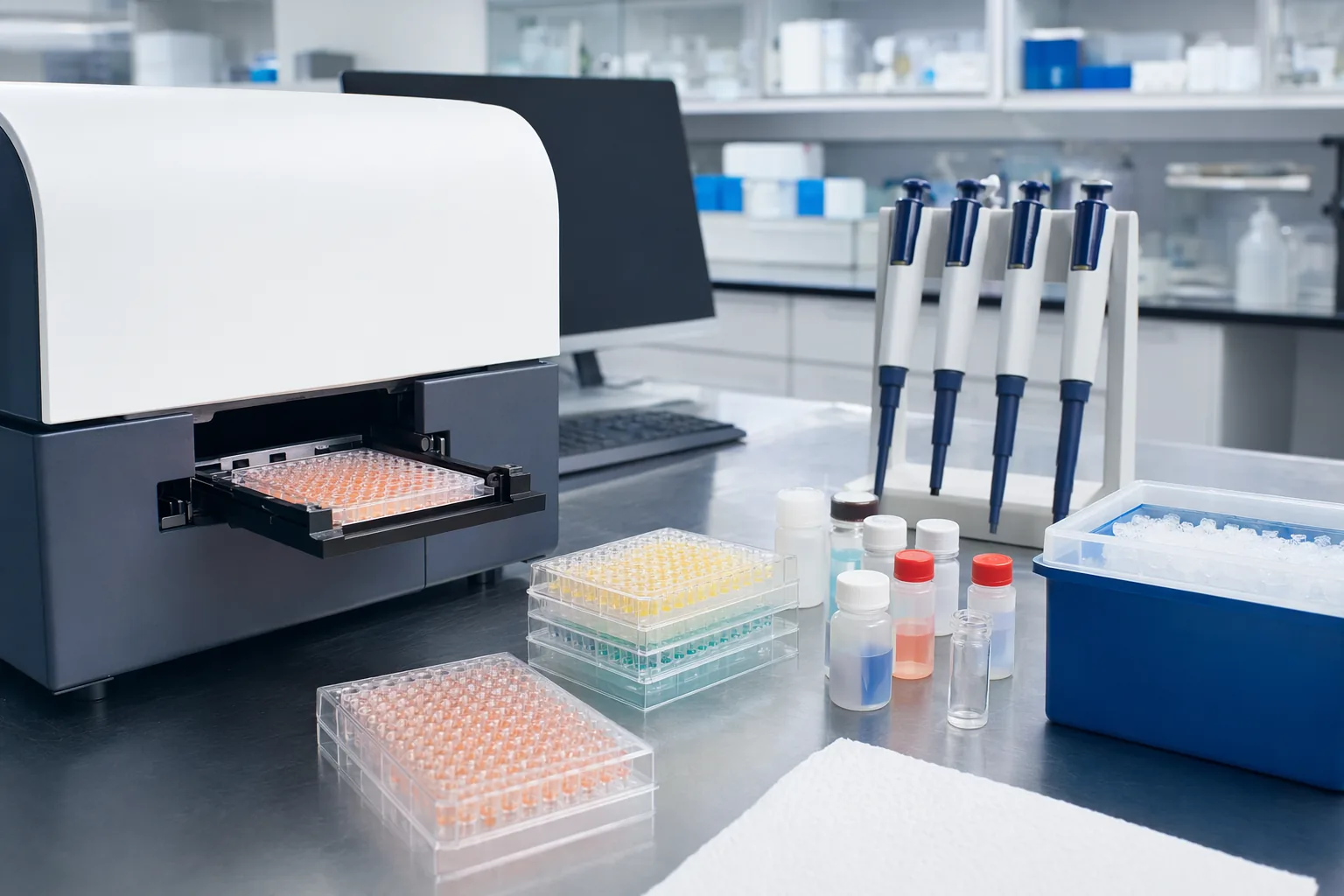
Wybieraj HRP i powiązane enzymy do ELISA z dokumentacją, kontrolą partii i wsparciem aplikacyjnym potrzebnym do powtarzalnej produkcji testów immunologicznych.
Dlaczego HRP pozostaje kluczowym enzymem do ELISA
Nadtlenaza chrzanowa jest szeroko stosowana w ELISA, ponieważ umożliwia czułe workflow kolorymetryczne, chemiluminescencyjne i szybkie oznaczenia punktu końcowego, gdy jest łączona z odpowiednimi substratami i właściwym projektem testu. Dla nabywców B2B decyzja zakupowa dotyczy mniej opisu katalogowego, a bardziej powtarzalności między partiami. Enzym HRP klasy diagnostycznej do ELISA powinien być oceniany pod kątem definicji aktywności, czystości, wpływu na tło, wydajności koniugacji, stabilności oraz zgodności z systemem blokującym, matrycą próbki i substratem. Pozyskiwanie przemysłowego enzymu HRP do ELISA wymaga także przewidywalnej dokumentacji i gotowości do skalowania. Nabywcy powinni potwierdzić, czy enzym jest przeznaczony do koniugacji, opracowania testu, produkcji zestawów czy wewnętrznych standardów QC, ponieważ każdy przypadek użycia może wymagać innych kryteriów akceptacji. Jeśli w zakresie znajdują się także formaty diagnostyczne z fosfatazą alkaliczną, należy porównać kinetykę enzymów, czas inkubacji, obsługę substratu i konfigurację czytnika przed standaryzacją platformy.
Typowa inkubacja ELISA: 20–37°C, zależnie od kinetyki antygen-przeciwciało. • Typowy warunek dla substratu HRP: system TMB w pobliżu pH 5.0–5.5. • Oceniaj stosunek sygnału do tła, a nie samą aktywność.
Kluczowe specyfikacje do wymagania przed zakupem
Wykwalifikowany dostawca enzymu HRP do ELISA powinien dostarczyć dokumenty przypisane do danej partii przed zatwierdzeniem produkcji. Poproś o COA z mierzoną aktywnością i testami zwalniającymi, TDS z informacjami o obsłudze i zalecanym przechowywaniu oraz SDS do bezpiecznego przyjęcia, magazynowania i szkolenia operatorów. Aktywność powinna być podana wraz z warunkami testu dostawcy, w tym substratem, pH, temperaturą i definicją jednostki, ponieważ wartości jednostek nie zawsze są porównywalne między metodami. Nabywcy powinni również sprawdzić stężenie białka, profil czystości, informację o stabilizatorze lub konserwancie, jeśli ma zastosowanie, wygląd, rozpuszczalność i warunki przechowywania. W programach koniugacji należy zapytać, czy klasa materiału nadaje się do sprzęgania z przeciwciałami oraz czy pozostałe zanieczyszczenia mogą wpływać na chemię znakowania. W produkcji zestawów należy potwierdzić dostępność reprezentatywnych partii pilotażowych i realistycznych wielkości partii produkcyjnych. Silna kwalifikacja dostawcy ogranicza ryzyko reformulacji i wspiera spójne zwalnianie enzymów ELISA w wielu kampaniach produkcyjnych.
Wymagaj COA, TDS, SDS i polityki retencji partii. • Potwierdź metodę testu i definicję jednostki przed porównaniem cen. • Poproś o materiał pilotażowy z docelowej ścieżki produkcyjnej.
Warunki procesu i walidacja pilotażowa
Walidacja pilotażowa powinna możliwie wiernie odzwierciedlać końcowy format ELISA, w tym typ płytki, bufor powlekania, reagent blokujący, chemię płukania, matrycę próbki, czas inkubacji, substrat, roztwór zatrzymujący i długość fali czytnika. W rozwoju koniugatu HRP należy przetestować molowe stosunki enzymu do przeciwciała, np. od 1:1 do 10:1, a następnie dopracować je na podstawie odzysku, tła i przyspieszonej stabilności. Dla koniugatów roboczych wiele programów rozpoczyna od szerokich ekranów rozcieńczeń, na przykład 1:2,000 do 1:50,000, zanim zawęzi zakres do dynamicznego przedziału testu. Temperatury reakcji wynoszą zwykle 20–25°C w rozwoju laboratoryjnym oraz 37°C tam, gdzie zweryfikowano szybsze wiązanie. Kontrole QC powinny obejmować tło próbki ślepej, odzysk niskiego dodatniego wyniku, ocenę efektu hook przy wysokich stężeniach, CV wewnątrzpłytkowe, porównanie między partiami oraz stabilność po symulacji transportu. Prace pilotażowe są również najlepszym etapem do pomiaru kosztu użycia, ponieważ droższy enzym klasy diagnostycznej może obniżyć dawkę, liczbę powtórzeń lub ryzyko reklamacji.
Prowadź testy równoległe partii przy tym samym czasie działania substratu. • Uwzględnij próbki z rzeczywistej matrycy, nie tylko kontrole buforowe. • Stosuj limity akceptacji powiązane z wymaganiami zwolnienia zestawu.
ELISA, kontekst radio-diagnostyczny i powiązane workflow enzymatyczne
Nabywcy czasem proszą dostawców o opisanie metod enzymatycznego testu immunoenzymatycznego ELISA radio-diagnostic methods przy porównywaniu platform immunoanalizy. ELISA wykorzystuje detekcję znakowaną enzymatycznie, taką jak HRP lub fosfataza alkaliczna, natomiast metody radio-diagnostyczne opierają się na znacznikach radioaktywnych i specjalistycznych kontrolach promieniowania. Konsekwencje zakupowe są różne: pozyskiwanie enzymów do ELISA koncentruje się na aktywności katalitycznej, zachowaniu podczas koniugacji, zgodności z substratem, przechowywaniu i ciągłości partii. Ogólna diagnostyka enzymatyczna może obejmować także enzymy biologii molekularnej, ale HRP nie należy do tej samej kategorii co enzymy używane w diagnostycznym trawieniu restrykcyjnym. Jeśli laboratorium stosuje diagnostyczny test cięcia enzymem restrykcyjnym równolegle z produkcją testów immunologicznych, należy kwalifikować te odczynniki oddzielnie, z własnymi jednostkami aktywności, buforami, temperaturami inkubacji i kryteriami analizy fragmentów. Wartość testów enzymatycznych w diagnostyce mikrobiologicznej zależy od zwalidowanego projektu testu, odpowiednich kontroli i spójnej wydajności odczynników, a nie wyłącznie od nazwy enzymu.
Oddziel kwalifikację enzymów do ELISA od kwalifikacji enzymów restrykcyjnych. • Nie zastępuj specyfikacji HRP specyfikacjami dla enzymów do testów molekularnych. • Dopasuj QC odczynnika do workflow diagnostycznego.
Kwalifikacja dostawcy i dopasowanie handlowe
Niezawodna relacja z dostawcą powinna wspierać zarówno rozwój testu, jak i powtarzalną produkcję. Oceń zdolność dostawcy do zapewnienia stałych wielkości partii, wcześniejszego informowania o zmianach procesu, praktycznych terminów realizacji oraz odpowiedzi technicznych od personelu znającego produkcję testów immunologicznych. Poproś o historyczne dane partii, jeśli są dostępne, ale nie opieraj się na nieweryfikowalnych twierdzeniach ani niepotwierdzonych obietnicach wydajności. Kwalifikacja dostawcy powinna obejmować kontrolę dokumentów, obsługę reklamacji, identyfikowalność próbek, przydatność opakowania, uzasadnienie wysyłki w łańcuchu chłodniczym lub w temperaturze otoczenia oraz dostępność próbek archiwalnych do dochodzeń. Porównanie handlowe powinno opierać się na koszcie użycia, a nie wyłącznie na cenie za gram. W obliczeniach uwzględnij dawkę enzymu, wydajność koniugacji, straty podczas oczyszczania, rozcieńczenie robocze, odrzucone partie, powtórne testowanie, awarie stabilności, nakład pracy QC, fracht i ryzyko zapasów. W regulowanej produkcji diagnostycznej dopasuj specyfikacje zakupowe do wewnętrznych plików walidacyjnych przed zatwierdzeniem dostawcy, klasy, wielkości opakowania i wymagań dotyczących testów zwalniających.
Porównuj koszt dostarczenia, dawkę, wydajność i potrzebę powtórnych testów. • Określ oczekiwania dotyczące powiadamiania o zmianach w warunkach zakupu. • Zakwalifikuj co najmniej jedną strategię zapasową, gdy ryzyko dostaw jest istotne.
Techniczna lista kontrolna zakupów
Pytania kupującego
Zacznij od końcowego formatu testu, a nie wyłącznie od ceny enzymu. Zdefiniuj planowane zastosowanie, system substratu, temperaturę inkubacji, okno sygnału, limit tła i docelową stabilność. Następnie porównuj kandydatów na partiach przy użyciu tych samych płytek, blokad, próbek i czytników, które są stosowane w produkcji. Poproś o dokumenty COA, TDS i SDS, zweryfikuj metodę oznaczania aktywności i oblicz koszt użycia po uzyskaniu danych o wydajności koniugacji i częstości powtórzeń.
Ważne kontrole QC obejmują aktywność według zdefiniowanej metody, profil czystości, stężenie białka, wygląd, rozpuszczalność i stabilność przechowywania. W zastosowaniu ELISA dodaj testy funkcjonalne: stosunek sygnału do tła, odzysk niskiego dodatniego wyniku, odpowiedź próbki ślepej, precyzję, porównywalność między partiami, interferencję matrycy i czas działania substratu. Najlepsza specyfikacja to zwykle połączenie testów zwalniających dostawcy i Twoich wewnętrznych kryteriów akceptacji specyficznych dla testu.
Nie automatycznie. Systemy diagnostyczne oparte na HRP i fosfatazie alkalicznej wykorzystują różne substraty, warunki pH, kinetykę, profile tła i okna detekcji. HRP jest często wybierany do szybkiego rozwoju barwy z TMB, podczas gdy workflow z fosfatazą alkaliczną zwykle działa przy zasadowym pH i może lepiej odpowiadać innym wymaganiom stabilności lub sygnału. Zmiana enzymu wymaga ponownej optymalizacji rozcieńczenia koniugatu, czasu inkubacji, substratu, chemii zatrzymania i limitów zwalniania testu.
Koszt użycia oznacza rzeczywisty koszt uzyskania akceptowalnych wyników testu, a nie tylko cenę zakupu enzymu. Obejmuje dawkę enzymu, wydajność koniugacji, straty podczas oczyszczania, rozcieńczenie robocze, nieudane partie, powtórne testowanie, awarie stabilności, pracę QC, fracht i ryzyko zapasów. Enzym klasy diagnostycznej o wyższej cenie jednostkowej może być handlowo lepszy, jeśli zapewnia niższe tło, dłuższą stabilność lub bardziej spójną wydajność partii.
To sformułowanie zwykle odzwierciedla pytanie edukacyjne lub egzaminacyjne porównujące ELISA z metodami radio-diagnostycznymi. W zakupach kluczowe jest praktyczne rozróżnienie: ELISA opiera się na znacznikach enzymatycznych, takich jak HRP lub fosfataza alkaliczna, natomiast formaty radio-diagnostyczne wykorzystują odczynniki znakowane radioaktywnie i inne kontrole. Nabywcy przemysłowi powinni koncentrować się na zwalidowanej wydajności enzymu, dokumentacji, zgodności z substratem, spójności partii i kwalifikacji dostawcy dla swojego konkretnego testu immunologicznego.
HRP jest enzymem reporterowym do testów immunologicznych, natomiast enzymy restrykcyjne tną kwasy nukleinowe w określonych sekwencjach w workflow molekularnych. Stosowanie diagnostycznego testu cięcia enzymem restrykcyjnym wymaga innych specyfikacji, takich jak sekwencja rozpoznawana, bufor, temperatura trawienia, definicja jednostki i analiza fragmentów. HRP należy kwalifikować do generowania sygnału ELISA; enzymy restrykcyjne należy kwalifikować oddzielnie pod kątem wydajności testów molekularnych.
Powiązane tematy wyszukiwania
przemysłowy enzym hrp do elisa, dostawca enzymu hrp do elisa, opisz enzymatyczny test immunoenzymatyczny elisa radio-diagnostic methods, 20 opisz enzymatyczny test immunoenzymatyczny elisa radio-diagnostic methods, ogólna diagnostyka enzymatyczna, diagnostyczne trawienie enzymem restrykcyjnym
Diagnostic Enzymes (ELISA & Assay Grade) for Research & Industry
Need Diagnostic Enzymes (ELISA & Assay Grade) for your lab or production process?
ISO 9001 certified · Food-grade & research-grade · Ships to 80+ countries
Najczęściej zadawane pytania
Jak wybrać enzym HRP do produkcji zestawów ELISA?
Zacznij od końcowego formatu testu, a nie wyłącznie od ceny enzymu. Zdefiniuj planowane zastosowanie, system substratu, temperaturę inkubacji, okno sygnału, limit tła i docelową stabilność. Następnie porównuj kandydatów na partiach przy użyciu tych samych płytek, blokad, próbek i czytników, które są stosowane w produkcji. Poproś o dokumenty COA, TDS i SDS, zweryfikuj metodę oznaczania aktywności i oblicz koszt użycia po uzyskaniu danych o wydajności koniugacji i częstości powtórzeń.
Jakie testy QC są najważniejsze przy wyborze enzymu klasy diagnostycznej?
Ważne kontrole QC obejmują aktywność według zdefiniowanej metody, profil czystości, stężenie białka, wygląd, rozpuszczalność i stabilność przechowywania. W zastosowaniu ELISA dodaj testy funkcjonalne: stosunek sygnału do tła, odzysk niskiego dodatniego wyniku, odpowiedź próbki ślepej, precyzję, porównywalność między partiami, interferencję matrycy i czas działania substratu. Najlepsza specyfikacja to zwykle połączenie testów zwalniających dostawcy i Twoich wewnętrznych kryteriów akceptacji specyficznych dla testu.
Czy HRP można zamiennie stosować z fosfatazą alkaliczną w ELISA?
Nie automatycznie. Systemy diagnostyczne oparte na HRP i fosfatazie alkalicznej wykorzystują różne substraty, warunki pH, kinetykę, profile tła i okna detekcji. HRP jest często wybierany do szybkiego rozwoju barwy z TMB, podczas gdy workflow z fosfatazą alkaliczną zwykle działa przy zasadowym pH i może lepiej odpowiadać innym wymaganiom stabilności lub sygnału. Zmiana enzymu wymaga ponownej optymalizacji rozcieńczenia koniugatu, czasu inkubacji, substratu, chemii zatrzymania i limitów zwalniania testu.
Co oznacza koszt użycia przy zakupie enzymów do ELISA?
Koszt użycia oznacza rzeczywisty koszt uzyskania akceptowalnych wyników testu, a nie tylko cenę zakupu enzymu. Obejmuje dawkę enzymu, wydajność koniugacji, straty podczas oczyszczania, rozcieńczenie robocze, nieudane partie, powtórne testowanie, awarie stabilności, pracę QC, fracht i ryzyko zapasów. Enzym klasy diagnostycznej o wyższej cenie jednostkowej może być handlowo lepszy, jeśli zapewnia niższe tło, dłuższą stabilność lub bardziej spójną wydajność partii.
Dlaczego w niektórych wyszukiwaniach pojawia się fraza „20 describe enzyme linked immunosorbent assay ELISA radio-diagnostic methods”?
To sformułowanie zwykle odzwierciedla pytanie edukacyjne lub egzaminacyjne porównujące ELISA z metodami radio-diagnostycznymi. W zakupach kluczowe jest praktyczne rozróżnienie: ELISA opiera się na znacznikach enzymatycznych, takich jak HRP lub fosfataza alkaliczna, natomiast formaty radio-diagnostyczne wykorzystują odczynniki znakowane radioaktywnie i inne kontrole. Nabywcy przemysłowi powinni koncentrować się na zwalidowanej wydajności enzymu, dokumentacji, zgodności z substratem, spójności partii i kwalifikacji dostawcy dla swojego konkretnego testu immunologicznego.
Czym HRP różni się od enzymów używanych w diagnostycznym teście cięcia enzymem restrykcyjnym?
HRP jest enzymem reporterowym do testów immunologicznych, natomiast enzymy restrykcyjne tną kwasy nukleinowe w określonych sekwencjach w workflow molekularnych. Stosowanie diagnostycznego testu cięcia enzymem restrykcyjnym wymaga innych specyfikacji, takich jak sekwencja rozpoznawana, bufor, temperatura trawienia, definicja jednostki i analiza fragmentów. HRP należy kwalifikować do generowania sygnału ELISA; enzymy restrykcyjne należy kwalifikować oddzielnie pod kątem wydajności testów molekularnych.
Gotowy do pozyskania?
Przekształć ten przewodnik w brief dla dostawcy. Poproś o próbki enzymu HRP, przegląd COA/TDS/SDS oraz wsparcie partii pilotażowej dla swojego programu ELISA.
Contact Us to Contribute